qCART™
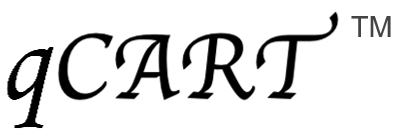
克服CAR-T細胞治療的挑戰
嵌合抗原受體T細胞(CAR-T)療法是癌症治療領域的重要突破,並且也已經在特定血癌中展現顯著的臨床療效。然而,若要將CAR-T細胞療法廣泛應用於多種癌症,仍需要克服些許挑戰,包括:(1) 毒性 來自標靶正確錯誤目標(On-target/off-tumor)或是細胞激素釋放症候群(Cytokine release syndrome, CRS);(2) 疾病復發 來自(i) 抗體逃逸和/或腫瘤抗原異質性,造成未被CAR-T細胞辨識的腫瘤細胞增生 (ii) CAR-T細胞維持性不足;(3) 效力不足 ,難以對抗實體腫瘤;以及(4) 高昂成本 於製備高品質CAR-T細胞。
在含有高比例的TSCM 細胞族群的CAR-T產品能夠有助於提升臨床療效,TSCM 細胞擁有幹性,可以高度自我更新能力,有助於維持長期穩定。此外TSCM 細胞因其優越的代謝適性以及較低的老化、衰竭程度,被認為是具有最強的治療潛力的細胞族群(圖1).
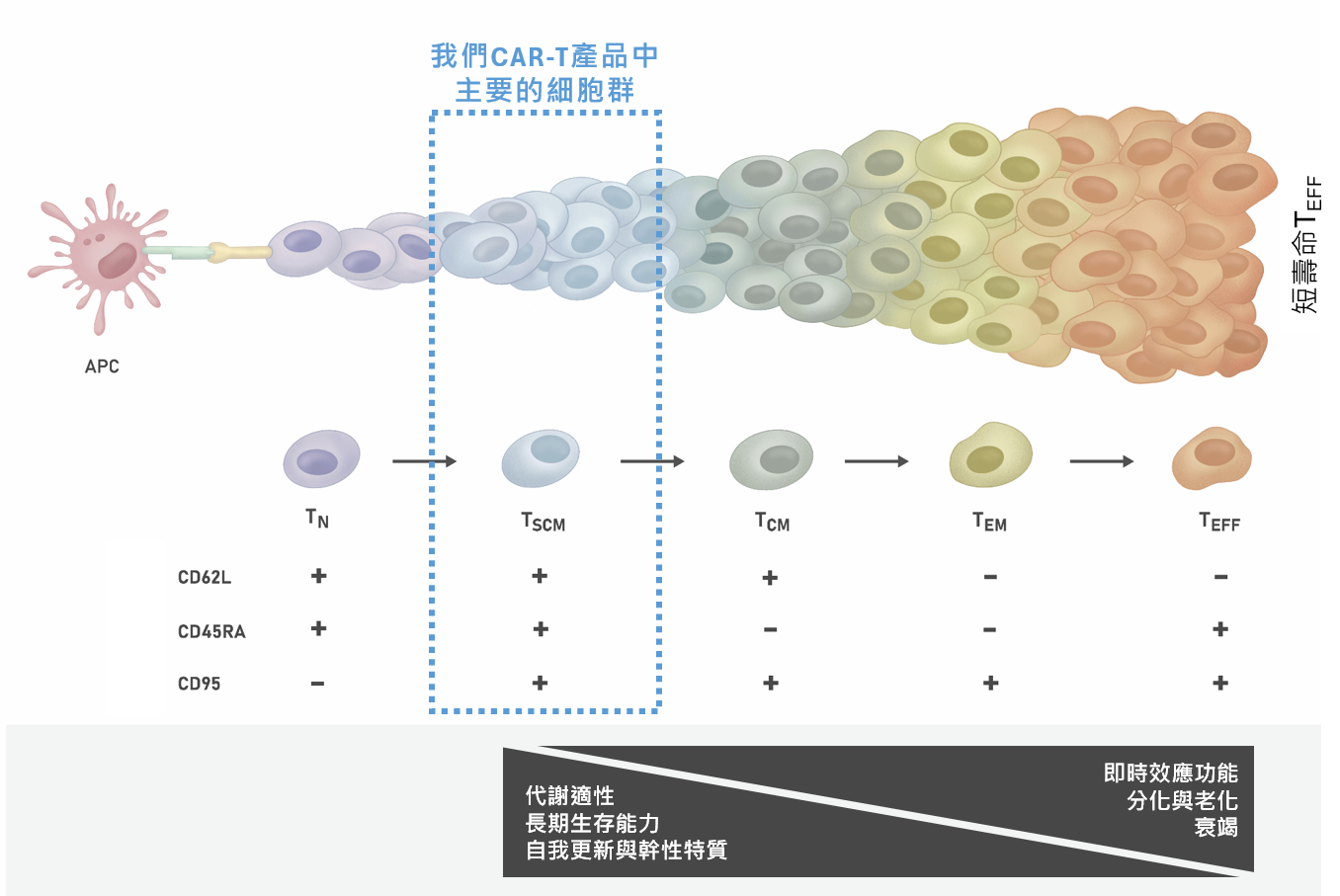
圖1. T細胞於抗原刺激下的分化階段
當初始T細胞 (Naïve T cell, TN )受到腫瘤相關抗原活化(可藉由抗原呈現細胞或APC),會產生長壽命的幹記憶T細胞(Stem cell-like memory T cell, TSCM )和中央記憶T細胞(Central memory T cell, TCM ),這些具有自我更新能力的T細胞會進一步分化為具有增殖能力的短壽命效應記憶T細胞(Effector memory T cell , TEM )和中央記憶T細胞(Central memory T cell, TEFF ) 。TSCM 細胞在其中被認為是最具治療潛力的T細胞族群。
CAR-T細胞在治療實體腫瘤的應用仍然面臨多項挑戰,包含(1) 缺乏CAR-T細胞追蹤至腫瘤部位;(2)實體腫瘤抗原特異性;以及(3)具有免疫抑制的腫瘤微環境(Tumor microenvironment, TME),會不利於T細胞功能表現(例如使T細胞分化、衰竭、老化甚至降低存活率),為了克服這些障礙,急需技術上的一大突破。
病毒載體因其高效率的基因遞送能力、整合能力以及長期穩低基因表現,因此在CAR-T細胞療法的開發中被廣泛應用,然而使用病毒載體產生的CAR-T細胞仍存在多項限制,包括:(1)病毒相關的安全疑慮;(2)病毒載體的攜帶容量有限;(3)轉染後的CAR⁺ T細胞比率與擴增能力低;(4)CAR-T細胞維持度低;以及(5)高昂的CAR-T細胞製備成本。
非病毒載體系統可以克服上述大多數甚至所有問題,然而電穿孔仍然是造成細胞損傷的一大挑戰,為了使非病毒載體系統能有效運作,須具備以下三項關鍵條件:(1)高效穩定的基因遞送系統;(2)能有效整合多個基因至CAR-T細胞裡的系統;以及(3)能夠製備臨床規模CAR-T細胞且穩定擴增的培養系統。
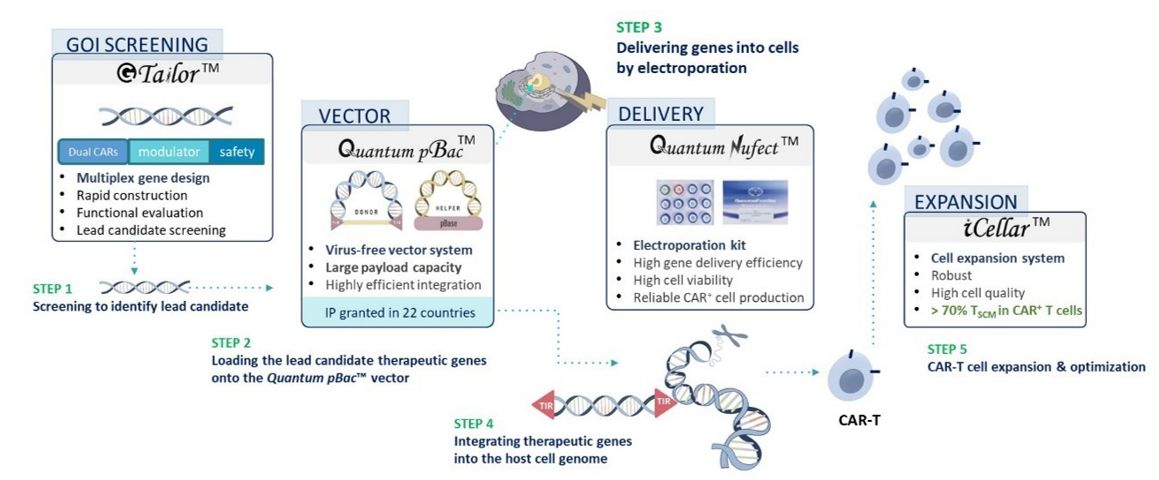
先驅生技 開發了 Quantum CART (qCART™)平台,一種非病毒的 Quantum Engine™ ,用於開發CAR-T細胞療法,整合四大核心技術,形成完整的解決方案:
(1) G-Tailor™:一套快速的多重基因設計、構築與篩選系統,能設計出以下特性的CAR-T細胞:(i)可同時辨識多種腫瘤抗原;(ii)攜帶促進CAR-T細胞追蹤至腫瘤和對抗腫瘤微環境的調節因子;以及(iii)內建安全開關,在需要時終止療程。
(2) Quantum Nufect™:高效率的基因遞送緩衝系統,可將目的基因遞送至T細胞,具備(i)可靠穩定的CAR-T細胞生產力,同時(ii)維持高度細胞活性。
(3) Quantum pBac™:非病毒載體系統,具備(i)整合大容量基因能力,和(ii)優先將基因整合至TSCM 細胞之基因體中。
(4) iCellar™:高效細胞擴增系統,可產出臨床規模的CAR-T細胞,具備(i)高比例的CAR⁺ TSCM 細胞,和(ii)優越的細胞適性及表現能力。
綜合上述四大平台, qCART™ 可以實現快速(約10天)、具成本效益以及臨床規模CAR-T製備(每升約1至3.5x109個細胞) (表1, 圖2 與 圖3).
非病毒的 qCART™ 平台可產出大量的臨床規模CAR-T細胞,其中含有高比例之CAR⁺ TSCM 細胞(表1),這些細胞具備高度毒殺腫瘤的活性 (圖2).
表1. 使用灌流式或補料式的培養條件,CAR-T細胞的製備比較
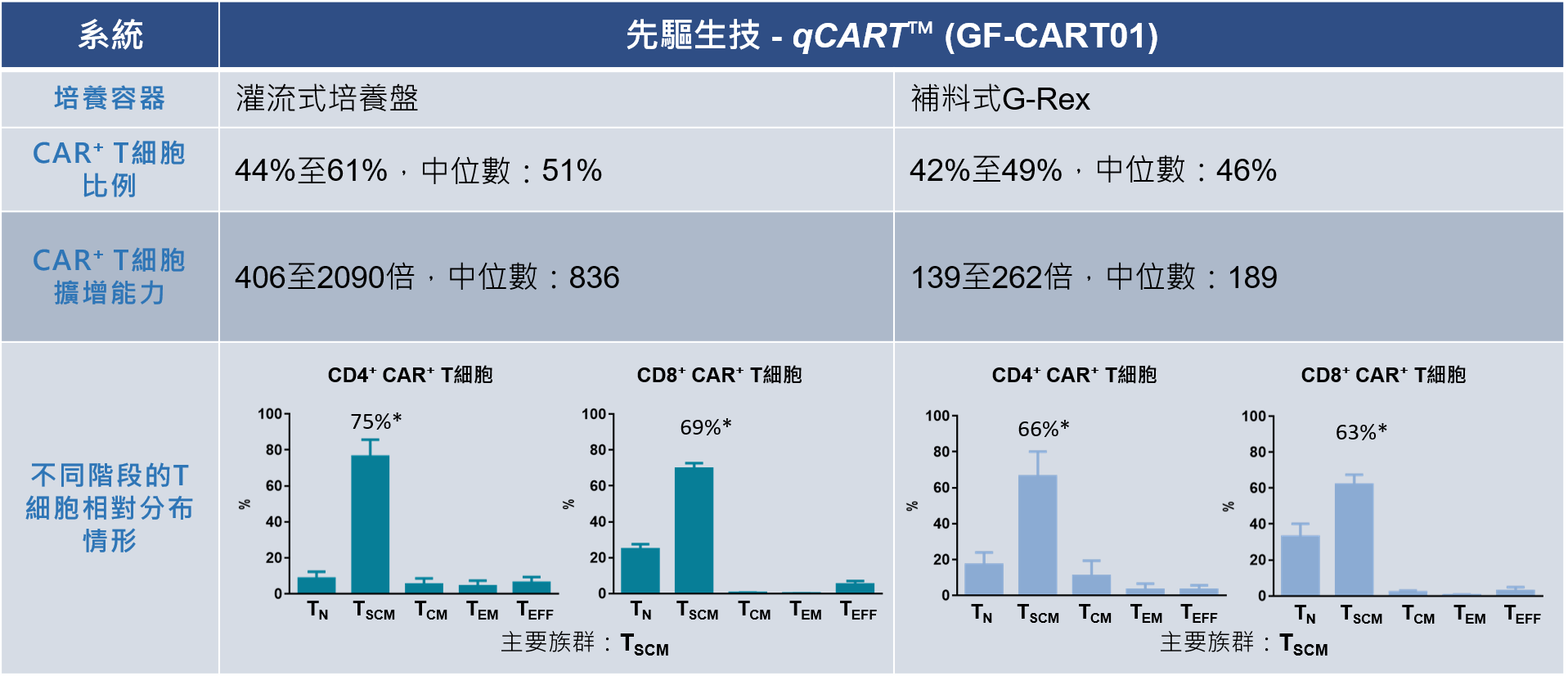
GF-CART01產品特性分析
CAR⁺ T細胞分別培養於傳統灌流式培養盤或補料式G-Rex。表中顯示CAR⁺ T細胞比例、細胞擴增倍數以及CD4⁺和CD8⁺ CAR⁺ T細胞亞群之數據分析,數據來自六位健康捐贈者。
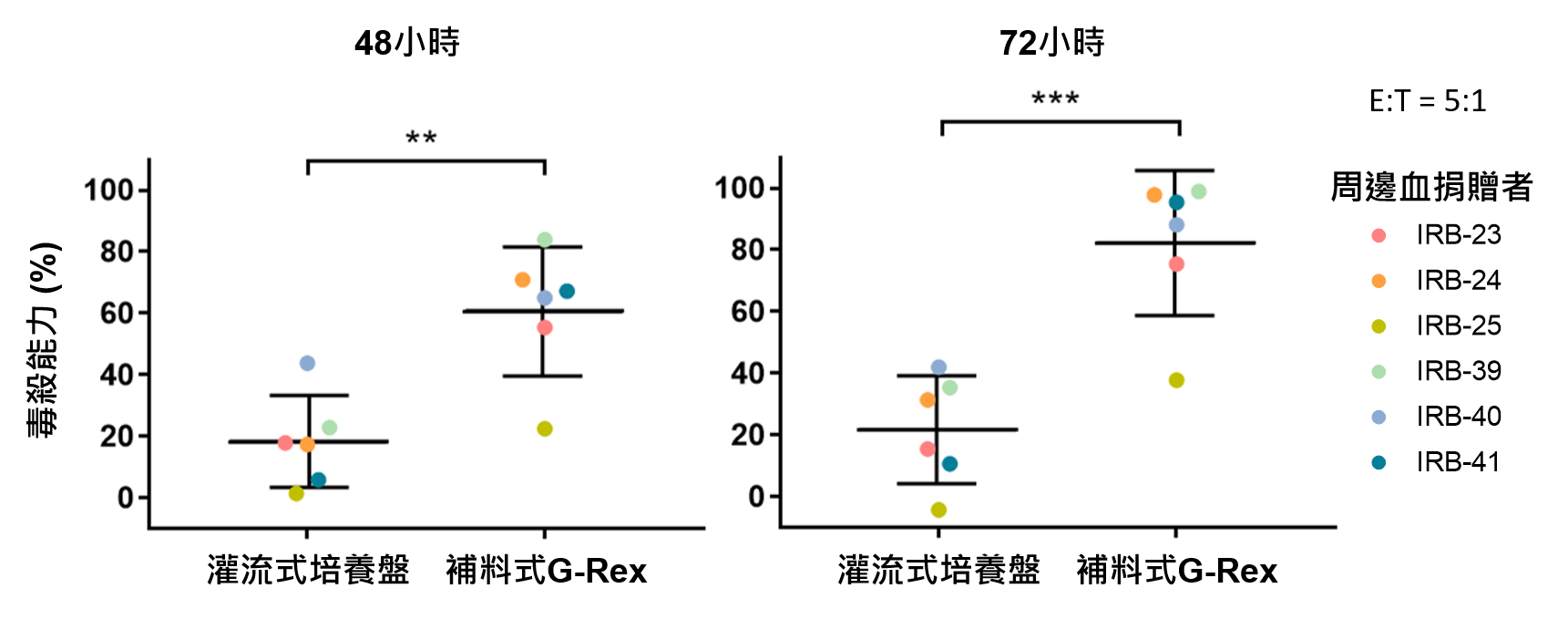
圖2. 使用G-Rex系統製備CAR-T細胞展現高度細胞毒殺活性
體外 功能分析:解凍後的CAR-T細胞經由Celigo影像細胞儀評估其殺傷活性,將CAR-T細胞與Raji-GFP/Luc的目標細胞共同培養48或72小時(CAR-T細胞數(E):目標細胞數(T) = 5:1),並觀察其細胞毒殺能力。數據來自六位健康捐贈者,橫線代表CAR-T細胞對目標細胞毒殺平均百分比。**p < 0.01; ***p < 0.001。
非病毒的 qCART™ 平台可穩定產出具高度擴增能力的CAR⁺ TSCM 細胞,無論其擁有不同標靶或是遞送基因大小差異 (表2),皆展現高度一致的製備效率,證明其具備開發多元CAR-T細胞構築的可能性。
表2. CAR-T細胞在不同標靶和不同遞送基因大小皆穩定表現